氨基酸是维持生命的基本单元,可相互结合生成肽进而合成蛋白质,从而介导细胞功能的发挥,包括免疫细胞。此外,氨基酸还被用于许多其他促进细胞和器官功能的过程,包括ATP的产生、核苷酸的合成以及氧化还原的平衡。免疫细胞对氨基酸有特定的需求,而生长因子刺激和T细胞激活可诱导其快速增殖,从而增加氨基酸转运蛋白的表达,表明该过程需要氨基酸摄取的增强。来自德国马克斯·普朗克免疫生物学和表观遗传学研究所的Beth Kelly和Erika L. Pearcel两位学者总结了氨基酸代谢促进免疫细胞功能的机制,并对靶向氨基酸代谢如何调节癌症、感染和自身免疫中的免疫反应进行了探讨。相关成果发表于《Cell Metabolism》。
氨基酸的获取与感知
每个氨基酸有其独特的侧链,从而具有不同的性质和功能。哺乳动物利用20种氨基酸进行蛋白质合成,当然在自然界中仍存在更多的氨基酸并影响细胞功能。这其中,9种必需氨基酸不能由人体自身充分合成而需从食物中获取,非必需氨基酸则相反,但在人体对氨基酸的需求超过合成能力时,也会成为必需氨基酸。这种依赖发生在快速增殖的细胞中,需要氨基酸合成蛋白质和增加生物量。鉴于细胞生长和增殖的显著变化是免疫细胞对细胞外环境变化的反应特征,对这些细胞来说,非必需氨基酸可能在免疫反应中成为条件必需的。
氨基酸获取是细胞功能的控制点。氨基酸从外部环境摄取依赖于转运蛋白,而在细胞内被循环利用并为其他氨基酸提供功能基团,如谷氨酰胺通过转氨和转酰胺作用为其他氨基酸提供氨基,蛋氨酸在蛋氨酸循环中代谢为半胱氨酸。溶酶体也含有氨基酸转运机制,可作为细胞内氨基酸库,对细胞功能很重要。溶酶体组氨酸转运蛋白Slc15a4是浆细胞样树突状细胞(pDCs)产生Toll样受体(TLR)诱导的I型干扰素(IFN-I)和B细胞产生IFN-I和免疫球蛋白(Ig)G所必需的。这种溶酶体氨基酸储存可能诱导自噬,从而促进长寿,部分是通过拮抗衰老相关CD8+T细胞功能的下降及对感染和癌症的免疫反应。溶酶体储存为细胞提供氨基酸库,当蛋白质合成恢复时,这些氨基酸可以被调动起来,而自噬可能在这种情况下增加氨基酸的可用性。氨基酸可以选择性地释放以驱动特定的基因表达程序,从而适应长期的饥饿或营养恢复,例如通过影响表观遗传修饰。
氨基酸转运蛋白调控免疫细胞功能。通过转运蛋白摄取氨基酸是一个严格调控的过程,对免疫细胞的激活和功能至关重要。不同类型免疫细胞表达的转运蛋白和受体的种类繁多,而CD4+和CD8+ T细胞的蛋白质组学分析阐明了抗原和细胞因子的刺激如何改变氨基酸转运蛋白的表达,从而改变营养摄取,特别是激活T细胞的效应功能。与未成熟的CD8+ T细胞相比,在细胞因子如白介素(IL)-2存在的情况下通过T细胞受体(TCR)激活的CD8+ T细胞会增加细胞表面Slc1a5和Slc7a5的密度。激活的T细胞需要氨基酸的供应来支持增殖,这种激活依赖的转运蛋白表达的增强保证了细胞可以根据需要获取这些营养物质。转运蛋白的表达水平也会影响T细胞功能。激活的CD4+和CD8+ T细胞表达类似的营养转运蛋白,CD4+ T细胞的转运蛋白拷贝数更低,营养转运更少。这一差异,以及相比CD8+ T细胞,活化的CD4+ T细胞的核糖体水平和翻译机制更低,可能是因为CD4+ T细胞比CD8+ T细胞的细胞质量和增殖能力更低。此外,经典和替代巨噬细胞的激活依赖于通过阳离子氨基酸转运蛋白(CAT)2 (Slc7a2)摄取的精氨酸,而静息状态的巨噬细胞可能是通过CAT1 (Slc7a1)利用y+ L (Slc7a6, Slc7a7)系统摄取精氨酸。可以说先天免疫细胞的激活依赖于氨基酸转运蛋白活性的重塑。
多种信号通路反过来控制转运蛋白的表达。Myc是一种驱动T细胞活化的中央转录因子,能增加CD4+和CD8+ T细胞的Slc1a5、Slc7a1、Slc7a5、Slc38a1和Slc38a2。Myc 缺乏通过降低这些转运蛋白的表达来阻断活化的T细胞生长。细胞因子对T细胞生长和增殖的不同影响是由转运蛋白的差异调控和信号通路的使用造成的。IL-2促进CD8+效应T (Teff)细胞的形成和生长,而IL-15则是体积较小的CD8+记忆T (Tmem )细胞的形成所必需的。与IL-15相比, IL-2刺激的T细胞有更高的CD98 (Slc7a5/Slc3a2)表达,并增加氨基酸摄取和蛋白质合成。这些作用依赖于IL-2培养的T细胞中持续的磷酸肌醇-3-激酶(PI3K)信号,而IL-15培养的细胞中则依赖更短暂的PI3K信号。当然仍需要更多的研究来了解细胞因子是如何通过调节氨基酸转运蛋白从而控制免疫细胞生长的信号通路活性和动力学。
氨基酸转运蛋白的不对称分布影响T细胞的命运。感染期间,T细胞群体必须产生Teff细胞来对抗感染,产生Tmem 细胞提供持久的免疫,不对称细胞分裂是T细胞实现这一目标的一种模型。在不对称细胞分裂过程中,子细胞不平等地遗传蛋白质、RNA和细胞器,为它们不同的命运奠定了基础。抗原呈递细胞(APCs)刺激未成熟T细胞的活化和增殖。基于因子(包括CD3、CD4、CD8、CD62L、转录因子和mTOR)的不对称遗传,子细胞之间,靠近APC的T细胞采用效应样命运,而远端T细胞采用记忆样命运。比如Slc1a5,优先聚集在近端细胞,也增加氨基酸丰度、谷氨酰胺摄取、糖酵解、c-Myc和mTOR复合物(mTORC)1活性。这里Slc1a5对c-Myc的直接作用尚未清晰,但氨基酸的剥夺或谷氨酰胺分解的阻断减少了子细胞之间c-Myc的差异,c-Myc水平的降低将子细胞推向记忆样表型。同样,Slc7a5表达升高的CD8+ T子细胞增加了CD8表达、mTORC1活性、Myc水平和糖酵解,而CD8和Slc7a5表达较低的细胞线粒体质量增加。因此,氨基酸代谢和细胞代谢特征是细胞命运的决定因素。
感知氨基酸调控免疫细胞代谢。mTORC1是一个驱动蛋白质合成、细胞生长和增殖的细胞信号中心,而GCN2激酶通过检测空载的tRNA来感知氨基酸饥饿。mTORC1仅在资源充分时才许可免疫细胞激活。活性mTORC1促进CD8+细胞毒性T细胞(CTLs)的分化,控制Tmem细胞形成,刺激Th1和Th17的分化,而限制Treg的形成。巨噬细胞中,药理上激活GCN2和氨基酸饥饿反应抑制IL-1β的产生以及炎性体介导的肠道炎症。一旦被激活,先天免疫细胞和适应性免疫细胞都必须感知其氨基酸供应,以参与伴随该激活的新的生物合成程序,在此情况下mTORC1和GCN2是氨基酸利用的主要调节者。
氨基酸支持免疫细胞代谢重编程
受体连接和细胞因子信号传导激活免疫细胞诱导转录和翻译发生剧烈变化产生细胞因子和效应分子,这需要获得生物量来进行细胞分裂。免疫细胞重编程其代谢来支持这些异常高的新陈代谢需求。ATP形式的能量是激活的免疫细胞的主要需求,糖酵解、TCA循环和OXPHOS协同产生ATP,而氨基酸调节这些相互连接的过程。氨基酸代谢促进糖酵解和TCA循环,以及线粒体脂肪酸氧化(FAO),进一步推动线粒体代谢和ATP的产生(图1)。
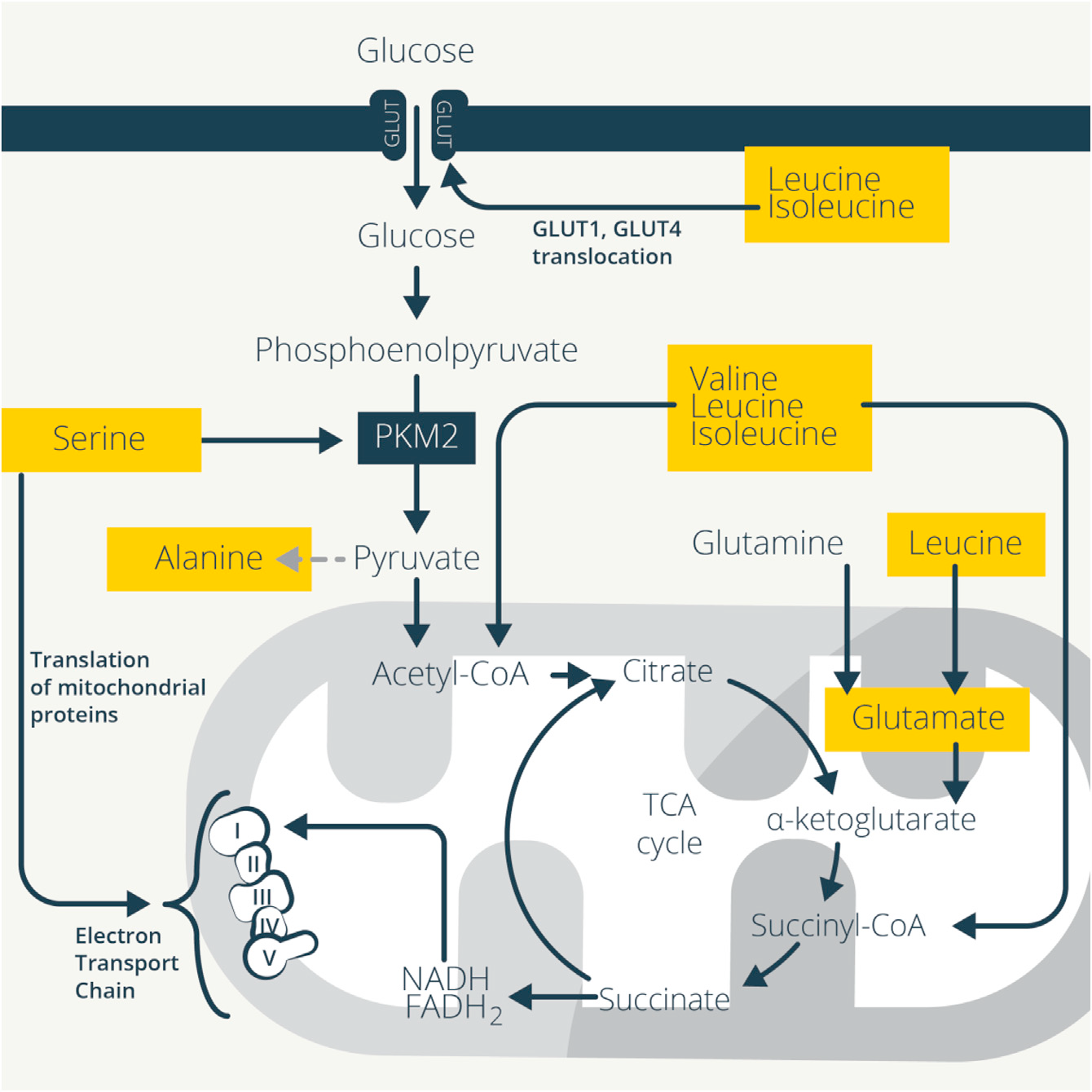
Figure 1. Amino Acids Support Glycolysis and Mitochondrial Metabolism
谷氨酰胺支持代谢重构。谷氨酰胺分解是增殖的细胞,包括激活的T细胞的主要能量产生过程。天门冬酰胺、脯氨酸或谷氨酸的补充可代谢为谷氨酰胺,但不会恢复由谷氨酰胺缺乏引起的增殖或细胞因子缺陷,表明胞外获得而非胞内产生的谷氨酰胺是关键的调节因素。这解释了为什么未成熟T细胞激活会诱导依赖于SNAT1, SNAT2 (Slc38a2) 和丙氨酸、丝氨酸、半胱氨酸偏好的转运蛋白2 (ASCT2;Slc1a5)的谷氨酰胺摄取。尽管增殖和IL-2的产生正常,ASCT2的破坏也会抑制Th1和Th17的分化。支持T细胞分化所必需的糖酵解和线粒体代谢的增加也在Asct2-/- / CD4+ T细胞中受损,因为它们降低了葡萄糖摄取、乳酸产生和耗氧量。补充谷氨酰胺可恢复这些作用,尽管ASCT2运输的其他氨基酸理论上也可能会导致这种表型。
谷氨酰胺支持Th1和Th17细胞的分化,但谷氨酰胺分解可能对Th17细胞更为关键,而谷氨酰胺的其他下游效应可能会影响Th1细胞的分化,这在缺乏谷氨酰胺酶1 (Gls1)的小鼠身上得到了证明。Gls1缺乏限制αKG的供应,损害Th17细胞的分化。Gls1中断抑制mTORC1和IL-2信号,进而抑制T细胞分化。同时,Gls1缺乏增加转录因子T-bet,促进Th1和CD8+ CTLs的分化和效应功能。限制谷氨酰胺分解可能增加其他过程的谷氨酰胺有效性,或者可能限制αKG产生支持T-bet介导的Th1细胞分化和功能的表观遗传特征。治疗上,Gls1抑制可改善实验性自身免疫脑脊髓炎(EAE)和类风湿关节炎模型的高炎症。谷氨酰胺分解是支持特定T细胞亚群功能的主要分解代谢途径。
不同免疫细胞类型具有不同的谷氨酰胺代谢。IL-2/IL -12诱导的Myc依赖性自然杀伤(NK)细胞的激活需要Slc7a5介导的谷氨酰胺摄取。这种情况下谷氨酰胺的获取而非降解是重要的,因为是谷氨酰胺剥夺而不是谷氨酰胺分解的阻断抑制NK细胞的激活。相反,谷氨酰胺分解支持激活的B细胞产生抗体。激活的B细胞中let-7adf microRNA簇过表达抑制ASCT2和Gls1的表达,减少IgM和IgG的产生。
谷氨酰胺对αKG的回补在促炎的M1样巨噬细胞中增加,并且TCA循环的中断导致琥珀酸的积累,驱动IL-1β的产生。一氧化氮(NO)介导的丙酮酸脱氢酶和乌头酸酶-2抑制限制了代谢产物进入TCA循环,促进炎症巨噬细胞中谷氨酰胺回补为αKG。谷氨酰胺流入TCA循环是IL-4诱导M2样巨噬细胞极化的原因。浆细胞也使用谷氨酰胺来替代缺乏的谷氨酸和天门冬氨酸。相比之下,活化的NK细胞使用谷氨酰胺来补充TCA循环中间产物并增加OXPHOS,但葡萄糖供应的柠檬酸-苹果酸穿梭在这些细胞中对TCA循环活性的驱动作用更大。NKT细胞兼具先天和适应性免疫细胞的特征,并且表达高度受限的TCR库,也需要谷氨酰胺来生存和增殖。很明显,许多免疫细胞增加了谷氨酰胺的摄取。谷氨酰胺分解支持其中一些免疫细胞的功能,而另一些则将谷氨酰胺导入其他代谢途径。增强对不同细胞类型中谷氨酰胺利用的了解,将使谷氨酰胺代谢在治疗中有更明确的靶向作用。
支链氨基酸(BCAAs)为TCA循环提供中间产物,乙酰CoA和琥珀酰CoA。亮氨酸转氨也会产生谷氨酸,通过αKG补充TCA循环。与谷氨酰胺转运蛋白类似,免疫细胞激活后,许多中性氨基酸转运蛋白增加。L型氨基酸转运蛋白1(LAT1;Slc7a5)很好地说明了氨基酸转运蛋白如何将病原体感染与免疫反应联系起来。在体内,李斯特菌感染增加了Slc7a5在T细胞的表达,而IL-2保持了这种表达,维持了对活化T细胞的持续BCAA供应。抑制Slc7a5阻碍IFN-γ和IL-17的生成以及Th1和 Th17细胞的发育,但Treg细胞发育正常。缺乏Slc7a5的T细胞不能经历激活所必需的mTORC1和Myc依赖的糖酵解增加。特别是,单独敲除Slc7a5很大程度上复制了Myc缺乏对活化的CD4+T细胞蛋白质组的影响,并损害T细胞的生长。单一转运蛋白的缺失具有强烈的影响,说明氨基酸转运和获取对T细胞功能的重要性。
Slc7a5也会引起巨噬细胞代谢重整。LPS增加巨噬细胞中BCAA转运蛋白的表达,并且缺乏Slc7a5介导的亮氨酸转运的巨噬细胞糖酵解和IL-1β的产生降低。CD98在分泌抗体的浆细胞中的表达较高,其缺失会影响抗体的产生。细胞表面CD98的表达与浆细胞寿命有关,高表面CD98水平的浆细胞比低表面CD98表达的短寿命浆细胞分泌更多的抗体。有趣的是,这些有着不同寿命的群体具有相似的转录谱,但代谢参数如CD98表达、葡萄糖摄取以及丙酮酸依赖的线粒体呼吸更能区分寿命差异的浆细胞。因此,操纵浆细胞代谢是增加体液免疫对病原体的持续时间的潜在有效的方法。
BCAA转氨酶(BCAT1)可将BCAA转化为支链α酮酸,链α酮酸再脱羧形成CoA衍生物。抑制BCAT1可限制糖酵解和耗氧量,以及抗炎物质衣康酸的产生。早期研究显示,喂养BCAAs缺失饮食小鼠产生缺陷抗体和细胞毒性T细胞反应,以响应鼠伤寒沙门氏菌或乳腺癌,而补充BCAAs可增强肝炎小鼠模型的肝脏CD8+ T活性,也可增加术后创伤或脓毒症患者淋巴细胞数量和对皮肤抗原的反应。缬氨酸促进肝硬化患者DC IL-12的产生。BCAA还可通过刺激葡萄糖摄取促进糖酵解以支持免疫细胞的代谢重编程。大鼠肌肉细胞中,亮氨酸和异亮氨酸可能依赖于PI3K和蛋白激酶C增加葡萄糖转运蛋白GLUT1和GLUT4向细胞表面的易位,以增加葡萄糖摄取。亮氨酸提供的乙酰CoA也可以乙酰化和激活mTORC1,进而增强糖酵解。
丝氨酸促进糖酵解,它连接和异构激活丙酮酸激酶M2(PKM2),在糖酵解最后一步将磷酸烯醇丙酮酸转化为丙酮酸。LPS诱导巨噬细胞中PKM2驱动代谢向糖酵解转变和IL-1β诱导。CD4+ T细胞的TCR刺激增加PKM2的核易位,这增强糖酵解以支持Th1和Th17细胞的生成、肿瘤坏死因子(TNF)和IL-17的产生。丝氨酸限制也抑制PKM2以减少动脉粥样硬化中巨噬细胞的过度激活,并且抑制丝氨酸合成可降低LPS诱导的内毒素血症中IL-1b和TNF的产生。
丝氨酸也促进线粒体代谢。线粒体翻译和呼吸作用需要丝氨酸羟甲基转移酶(Shmt2),Shmt2缺失的小鼠具有呼吸障碍,这种效应依赖于来自丝氨酸的一碳(1-C)单位的生成。线粒体翻译起始依赖于由丝氨酸通过Shmt2形成的修饰tRNA,N-甲酰甲硫氨酰tRNA(fMet-tRNAMet)。1-C单元的补充恢复了Shmt2缺乏的Jurkat细胞呼吸和线粒体翻译的缺陷。这条途径似乎在低糖条件下特别重要,可诱导细胞以补偿方式增加线粒体代谢,因此,它也可能对免疫细胞从糖酵解转向线粒体代谢很重要。然而,即使是有足够葡萄糖支持糖酵解增加的T细胞,OXPHOS和效应功能也依赖于丝氨酸下游的1-C代谢。甲基四氢叶酸脱氢酶2催化线粒体fMet-tRNAMet形成的中间步骤,生成NADH。在线粒体呼吸受损的胰腺组织中,这种NADH可以积累到有毒水平,从而抑制细胞生长。
虽然其他氨基酸可以为糖酵解和TCA循环提供原料,但有时T细胞并不用它们进行这些途径。胞外丙氨酸对T细胞早期激活是必需的,尽管丙氨酸可代谢为糖酵解的终产物丙酮酸,但它并不用于激活T细胞,反而用于蛋白质的合成。此外,虽然丙氨酸可以通过丙氨酸转氨酶从葡萄糖合成,但这种酶在激活早期的T细胞中的表达较低,细胞转而通过SNAT1吸收胞外丙氨酸。这保留了丙酮酸以供应乙酰CoA、TCA循环活性和OXPHOS,而胞外丙氨酸用于蛋白质合成。
氨基酸控制硫和氧化还原代谢
免疫细胞的激活往往取决于ROS的增加,LPS诱导巨噬细胞产生ROS从而驱动细胞因子的产生和杀菌。ROS可以激活活化的T细胞(NFAT)的核因子,增加T细胞的增殖。对未成熟B细胞的BCR刺激也会引起大量的ROS产生和钙诱导的线粒体功能障碍,这会导致激活诱导的细胞死亡,除非B细胞也接收了共刺激信号,如TLR或CD40参与。因此,细胞有多种抗氧化机制来控制ROS水平,氨基酸对于维持这些防御和氧化还原平衡至关重要(图2)。
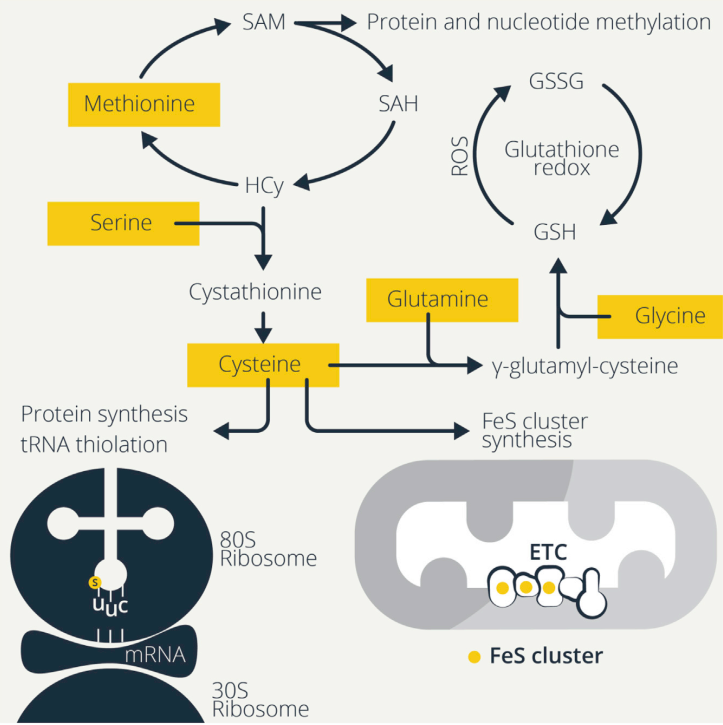
Figure2. Sulfurous Amino Acids Maintain Redox Balance and Drive Protein Synthesis
谷胱甘肽是T细胞和巨噬细胞功能所必需的。谷胱甘肽由甘氨酸、谷氨酸和半胱氨酸组成,因此,这些氨基酸的供应决定了谷胱甘肽水平。还原型谷胱甘肽(GSH)被氧化成为氧化谷胱甘肽(GSSG),谷胱甘肽还原酶(GSR)将GSSG重新还原为GSH,保持细胞内ROS解毒的GSH池。免疫细胞激活后ROS升高,增加了对GSH的需求,这就需要其组成氨基酸的供应。T细胞激活时GSH水平确实会增加,并且GSH从头合成而非GSSG循环对T细胞分化和功能的发挥具有重要作用。此外,谷胱甘肽还影响T细胞活化过程中糖酵解和谷氨酰胺利用率的增加。有条件的Gclc缺失消除了mTORC1的激活、NFAT的核积累以及激活的CD4+和CD8+T细胞中Myc依赖的向糖酵解和谷氨酰胺分解的代谢转变。这些细胞最初正常激活,但不能满足扩展的代谢需求而无法增殖。相反,GSH合成受损时,丝氨酸激活mTOR,从而抑制Foxp3的表达。丝氨酸限制可恢复Foxp3的表达和Treg细胞抑制活性,降低体内致死性自身炎症。因此,Treg细胞中GSH的一个功能是限制丝氨酸代谢,从而维持其抑制功能。巨噬细胞也利用丝氨酸为GSH产生甘氨酸,这是LPS诱导的IL-1βmRNA表达所必需的。这种丝氨酸-甘氨酸-GSH调节回路说明了氨基酸和小肽如何调节其他氨基酸的代谢。
半胱氨酸/胱氨酸导入部分通过促进GSH的合成支持免疫细胞功能。静息B细胞不表达xCT(Slc7a11),但激活后,增加xCT表达和胱氨酸的导入,可能是为产生GSH来对抗ROS的产生,否则会导致激活诱导的细胞死亡。DCs的LPS激活增加了系统XC-胱氨酸-谷氨酸抗逆向转运活性,这可能需要增加GSH的合成以对抗激活后ROS的增加。DCs还可以输出GSH来塑造细胞外氧化还原环境,特别是在DCs和T细胞之间的免疫突触周围。GSH分解为半胱氨酸,降低细胞外氧化还原电位以及促进CD4+ Teff细胞增殖,可能是因为CD4+ Teff细胞获得半胱氨酸用于GSH的产生和随后的增殖。此外,Treg细胞与DCs和CD4+ Teff细胞共培养耗尽细胞外半胱氨酸,这可能解释了Treg细胞对Teff细胞增殖的抑制作用。因此,天然免疫细胞调节氨基酸以调控适应性免疫细胞的功能。
半胱氨酸支持硫依赖的代谢。半胱氨酸是GSH功能发挥的关键氨基酸,因为硫的供应。半胱氨酸主要以其氧化形式,胱氨酸,存在于氧化细胞外环境中。胱氨酸的摄取对T细胞的激活、增殖和DNA合成是必需的。阻断T细胞对胱氨酸的摄取对EAE有保护作用。与B细胞相似,静息T细胞不表达xCT,但激活后表达xCT以促进胱氨酸的摄取。当胞外半胱氨酸供应有限时,蛋氨酸向半胱氨酸的转硫维持半胱氨酸依赖的过程。
半胱氨酸的硫供应对于通过合成铁硫(FeS)簇来维持线粒体代谢也是至关重要的。半胱氨酸脱硫酶NFS1从半胱氨酸中去除FeS簇的硫,并且半胱氨酸限制会降低FeS簇的合成。失去FeS簇本身会影响代谢途径,因为含有FeS簇的乌头酸酶不能再代谢柠檬酸,从而导致这种TCA循环中间体积累以及用于脂肪酸合成。精氨酸来源的NO破坏FeS的稳定性,表明NO可能拮抗M1样巨噬细胞线粒体代谢。此外,FeS簇合成的降低还会导致游离铁的过量,导致细胞铁死亡。胱氨酸-GSH通讯可调节氨基酸信号传导和铁死亡。
NFS1也会利用半胱氨酸的硫原子来生成硫醇化tRNA。赖氨酸、谷氨酰胺和谷氨酸tRNAs可以在摆动位点(U34)的尿苷酸上硫醇化,通过核糖体帮助tRNA易位来促进翻译。在硫限制,如蛋氨酸和半胱氨酸的限制过程中,这种tRNA硫醇化降低,在营养受限时翻译减弱。免疫细胞中,FeS簇合成与tRNA硫醇化尚未研究,但在这里可能会发挥作用,因为线粒体代谢的维持和翻译的增强是免疫细胞活化的基础。
参考文献
Kelly and Pearce, Amino Assets: How Amino Acids Support Immunity. Cell Metabolism (2020). https://doi.org/10.1016/j.cmet.2020.06.010.
原文阅读,请长按识别下方二维码

精彩推荐
2. Geroscience︱代谢组-微生物组-免疫因子关联分析揭示大鼠机体随年龄变化规律
3. Nature Reviews Clinical Oncology | 代谢调节提高免疫治疗
4. Immunity | 重磅综述: 饮食-菌群-免疫互作
5. TEM | 宿主与菌群互作的信号分子--AAA相关菌群代谢物
6. Cell子刊 | 癌细胞并不孤单--肿瘤微环境中的代谢通信

