
近年来,干细胞源性的小细胞外囊泡(sEVs)在各种疾病中的治疗作用得到广泛的关注。2020年,上海交通大学附属第六人民医院汪泱教授团队于J Extracell Vesicles发表的“Human ESC-sEVs alleviate age-related bone loss by rejuvenating senescent bone marrow-derived mesenchymal stem cells”文章中,发现胚胎干细胞源性细胞外囊泡中含有多种年轻化因子蛋白成分,并能够促进衰老小鼠骨髓间充质干细胞年轻化。此外,目前已有多项研究证实了sEVs治疗肌腱病变的潜在机制。值得关注的是,一些针对成体干细胞衍生的大细胞外囊泡(lEVs)的研究表明,lEVs可能实现与sEVs类似的治疗功能,而干细胞衍生的lEVs是否能够有效治疗肌腱病变尚不清楚。
2022年8月,汪泱教授团队在细胞外囊泡的研究中再次获得突破,于Bioactive Materials发表了题为“Large extracellular vesicles secreted by human iPSC-derived MSCs ameliorate tendinopathy via regulating macrophage heterogeneity“文章。文章研究了诱导性多能干细胞来源的间充质干细胞分泌的lEVs (iMSC-lEVs)在肌腱病变中的治疗作用以及iMSC-lEVs在体外对巨噬细胞极化的调节作用。通过外泌体蛋白质组学、RNA测序、蛋白免疫印迹等技术方法,研究表明iMSC-lEVs能够部分通过DUSP2和DUSP3来介导p38 MAPK信号通路,并使M1巨噬细胞向M2巨噬细胞进行极化转变,从而减轻肌腱病变中的疼痛和炎症。其中,中科新生命为该研究提供了细胞外囊泡蛋白质组学服务。

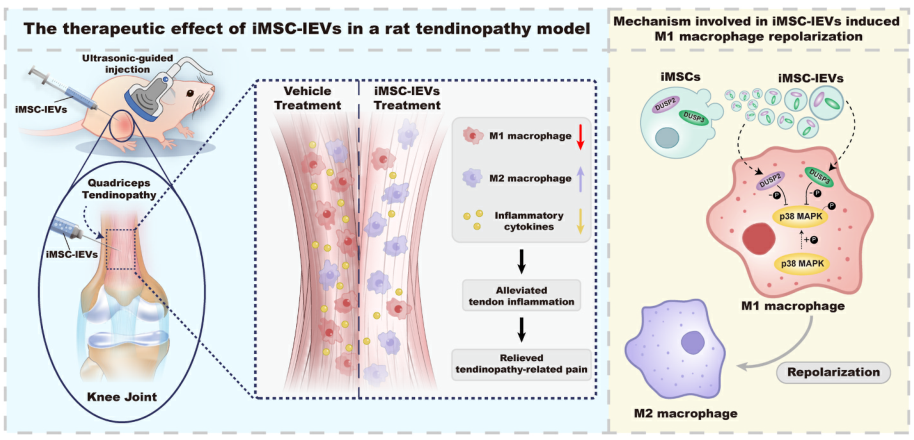
iMSC-lEVs在活体肌腱病变模型中的治疗机制及巨噬细胞复极调节机制示意图
研究材料
iMSC-lEVs;iMSC-sEVs;小鼠巨噬细胞细胞系RAW 264.7;大鼠肌腱病变模型;肌腱病患者肌腱组织
技术路线
- iMSC-sEVs和iMSC-lEVs的分离与表征;
- 建立大鼠肌腱病模型,并在体内评估iMSC-lEVs的镇痛作用;
- 采用RAW 264.7细胞,研究iMSC-lEVs对巨噬细胞极化的调节作用;
- RNA-seq方法探究iMSC-lEVs调节巨噬细胞表型改变的机制;
- 对iMSC-lEVs进行蛋白质组学分析以确定其调控通路的上游蛋白;
- 研究iMSC-lEVs对肌腱病患者肌腱组织的作用。
研究结果
- iMSC-sEVs和iMSC-lEVs的分离与表征
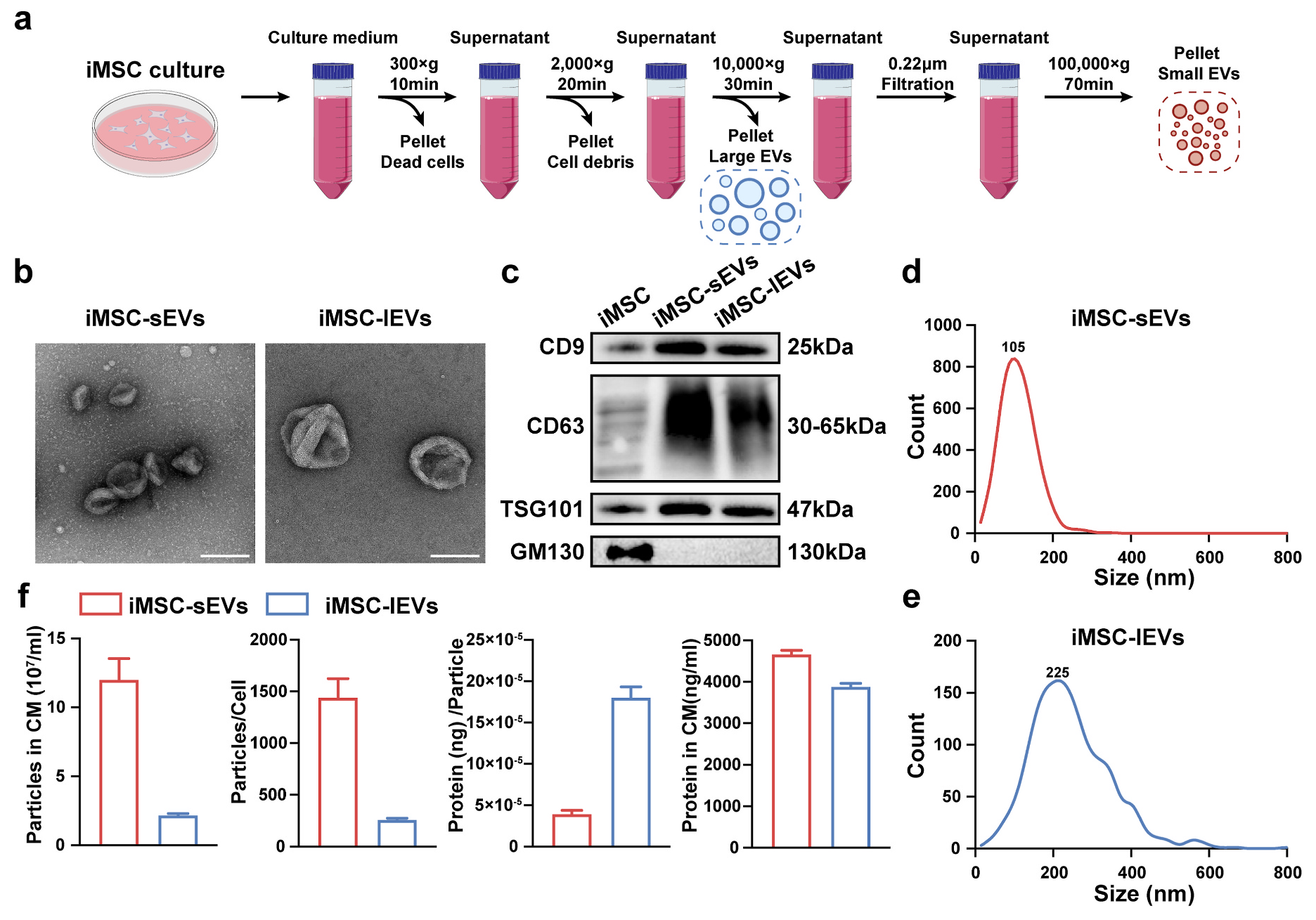
图1 iMSC-sEVs and iMSC-lEVs的分离与表征图
接下来研究人员研究了lEVs对巨噬细胞表型浸润的影响。 IHC染色结果显示,在治疗2周和4周后,lEVs治疗减少M1巨噬细胞的浸润,并促进M2巨噬细胞的浸润(图2d和e),且lEVs组与sEVs组无显著差异(M1巨噬细胞浸润可加重肌腱病相关疼痛,而M2巨噬细胞浸润可改善肌腱病相关疼痛)。免疫组化染色显示,治疗2周和4周后,lEVs和sEVs治疗均显著降低促炎因子的表达(图3a和b)。这些数据表明,lEVs治疗在大鼠肌腱病变模型中具有抗炎和镇痛作用,且与sEVs的能力相似。
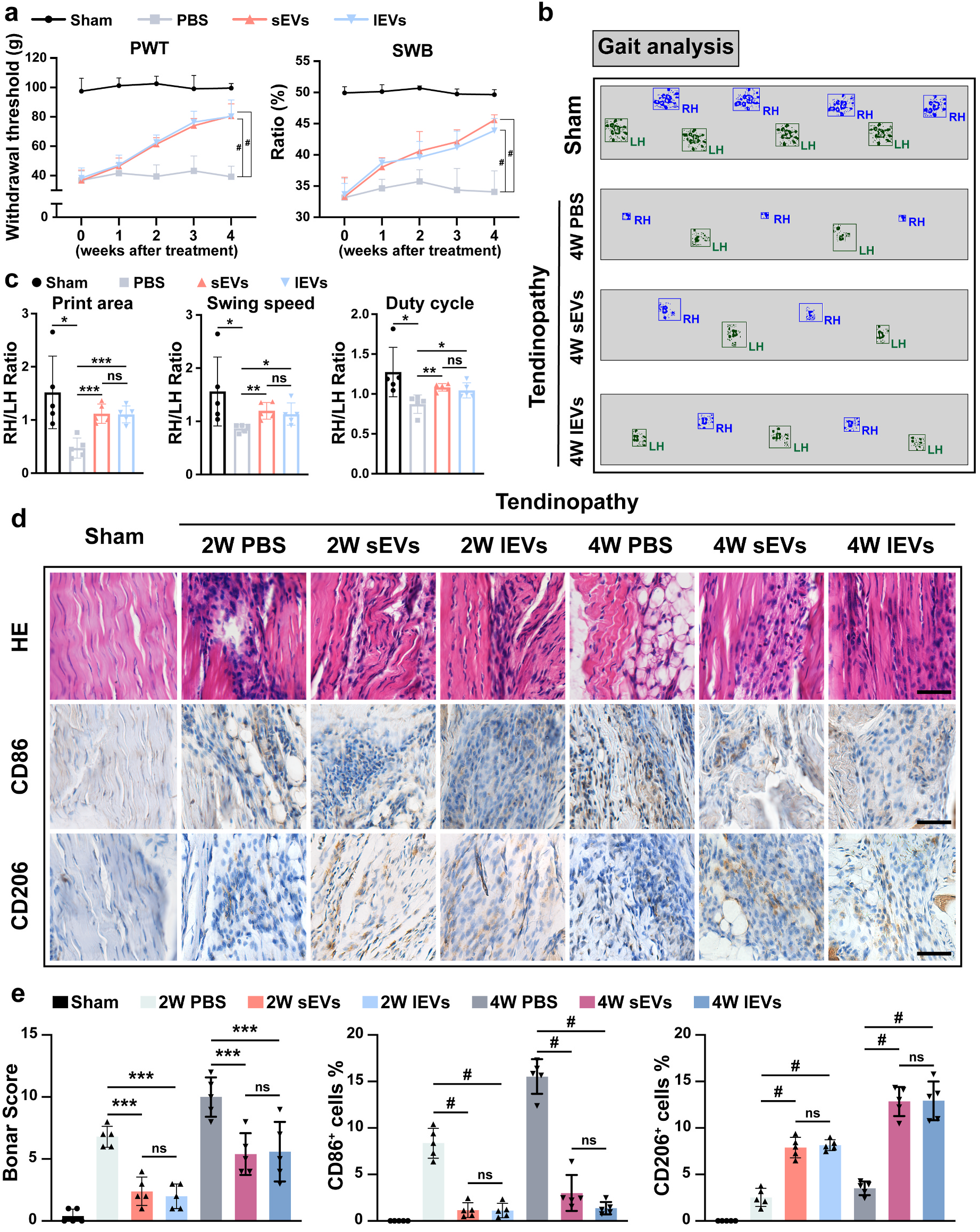
图2 iMSC-lEVs治疗可改善疼痛相关行为并调节体内巨噬细胞浸润
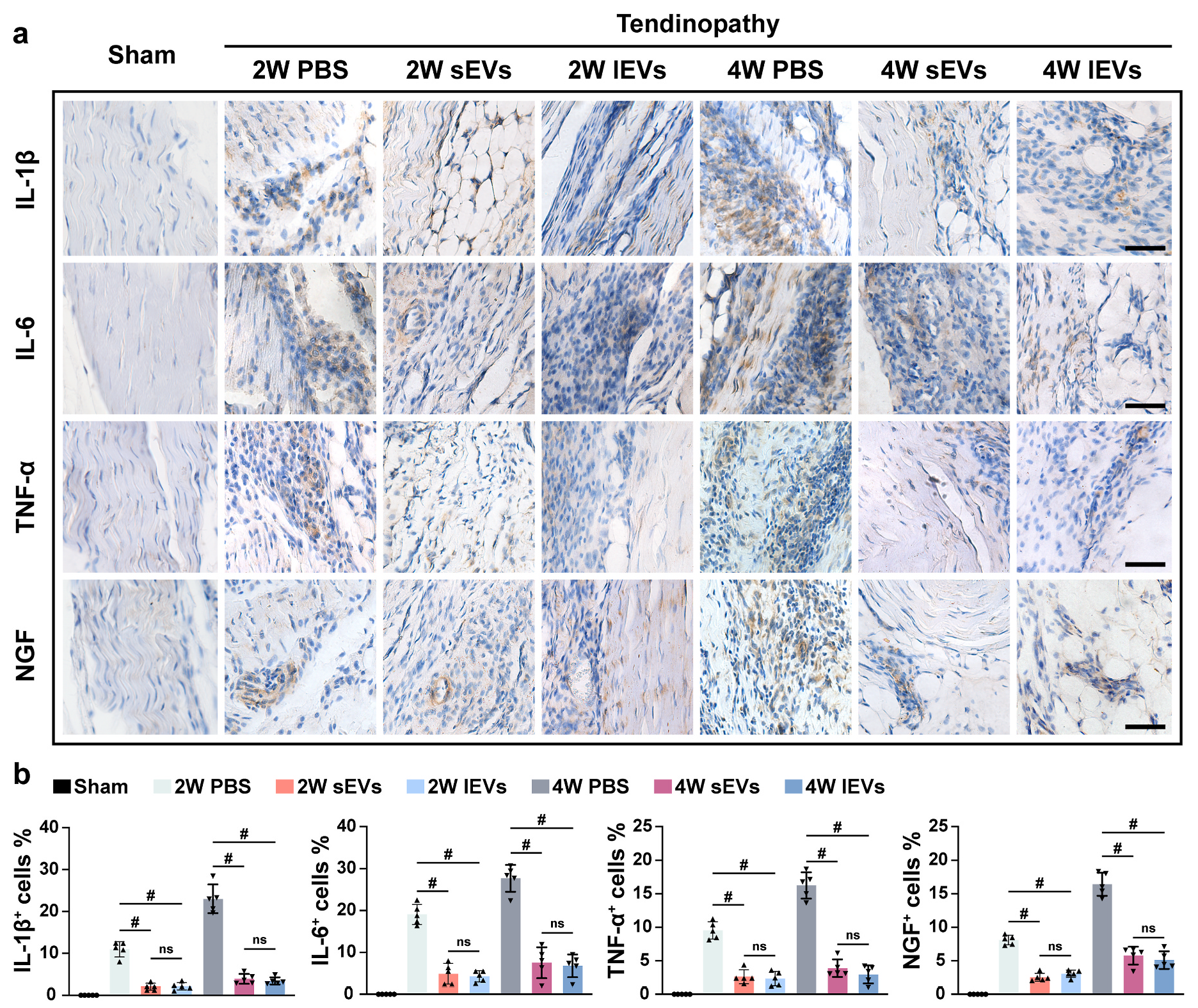
图3 iMSC-lEVs治疗降低大鼠体内炎症细胞因子表达
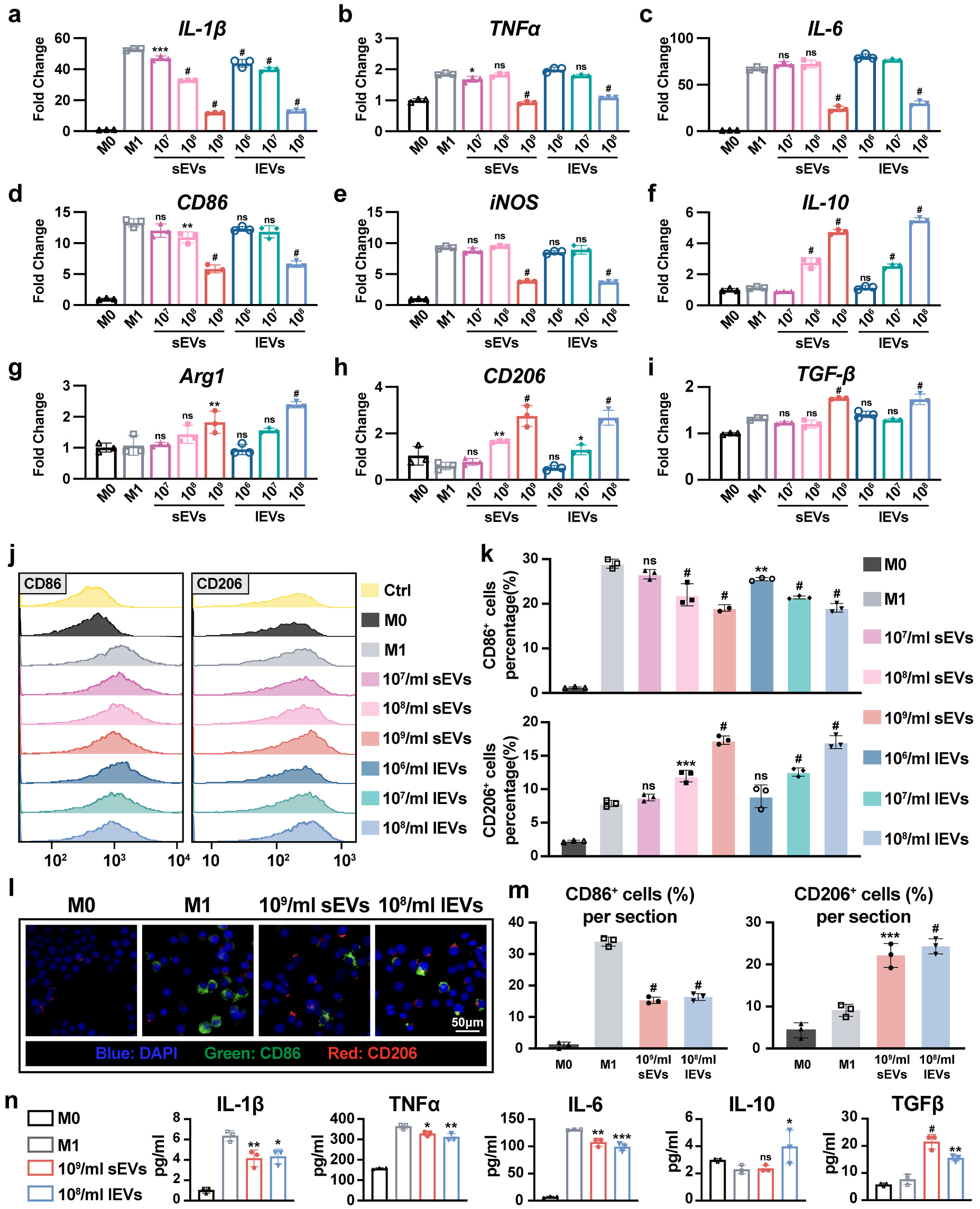
图4 iMSC-lEVs在体外以剂量依赖性的方式调节巨噬细胞极化
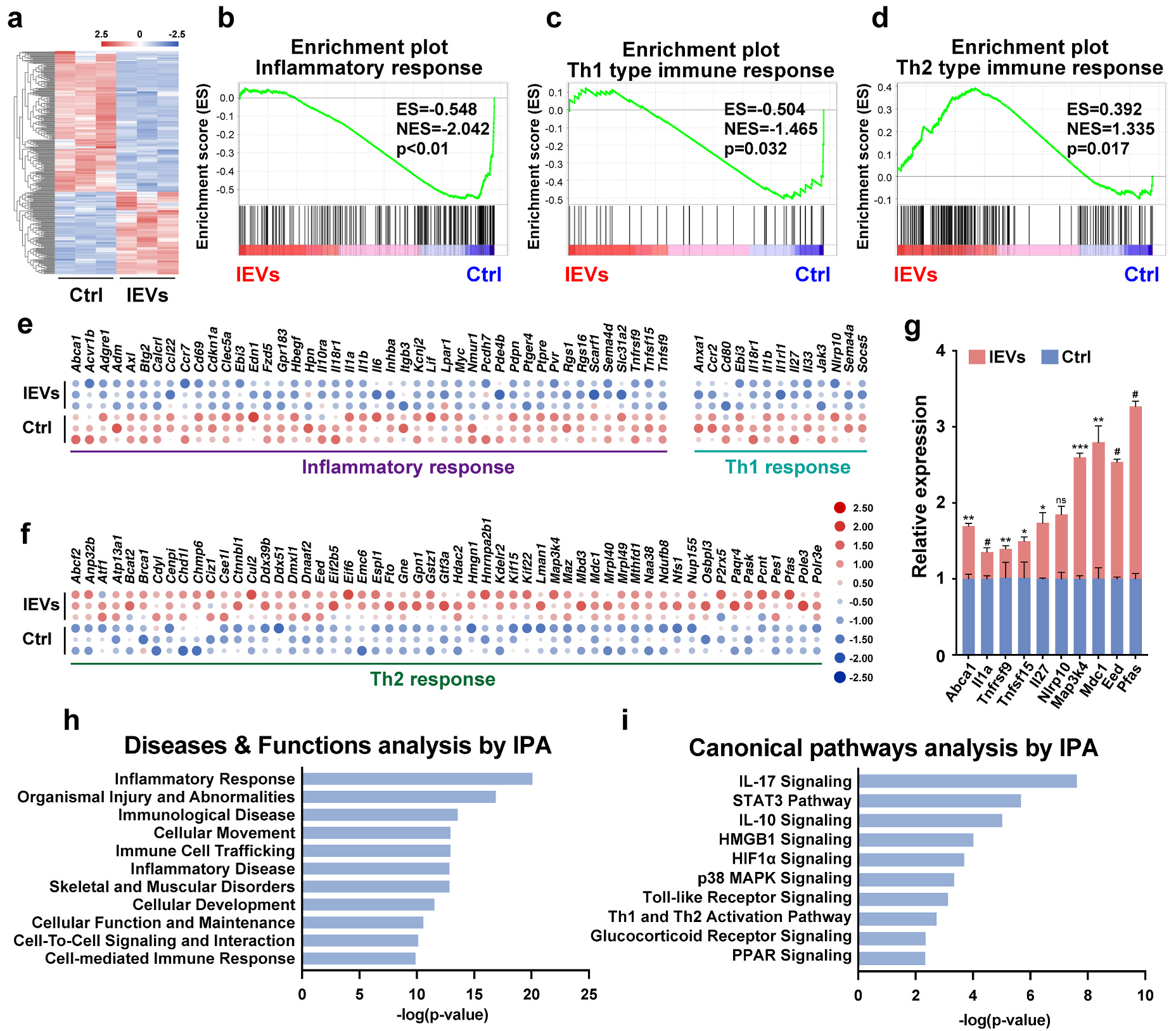
图5 RNA-seq分析LPS刺激的RAW 264.7细胞在iMSC-lEVs处理后的转录组变化
5.iMSC-lEVs可向巨噬细胞传递DUSP2和DUSP3
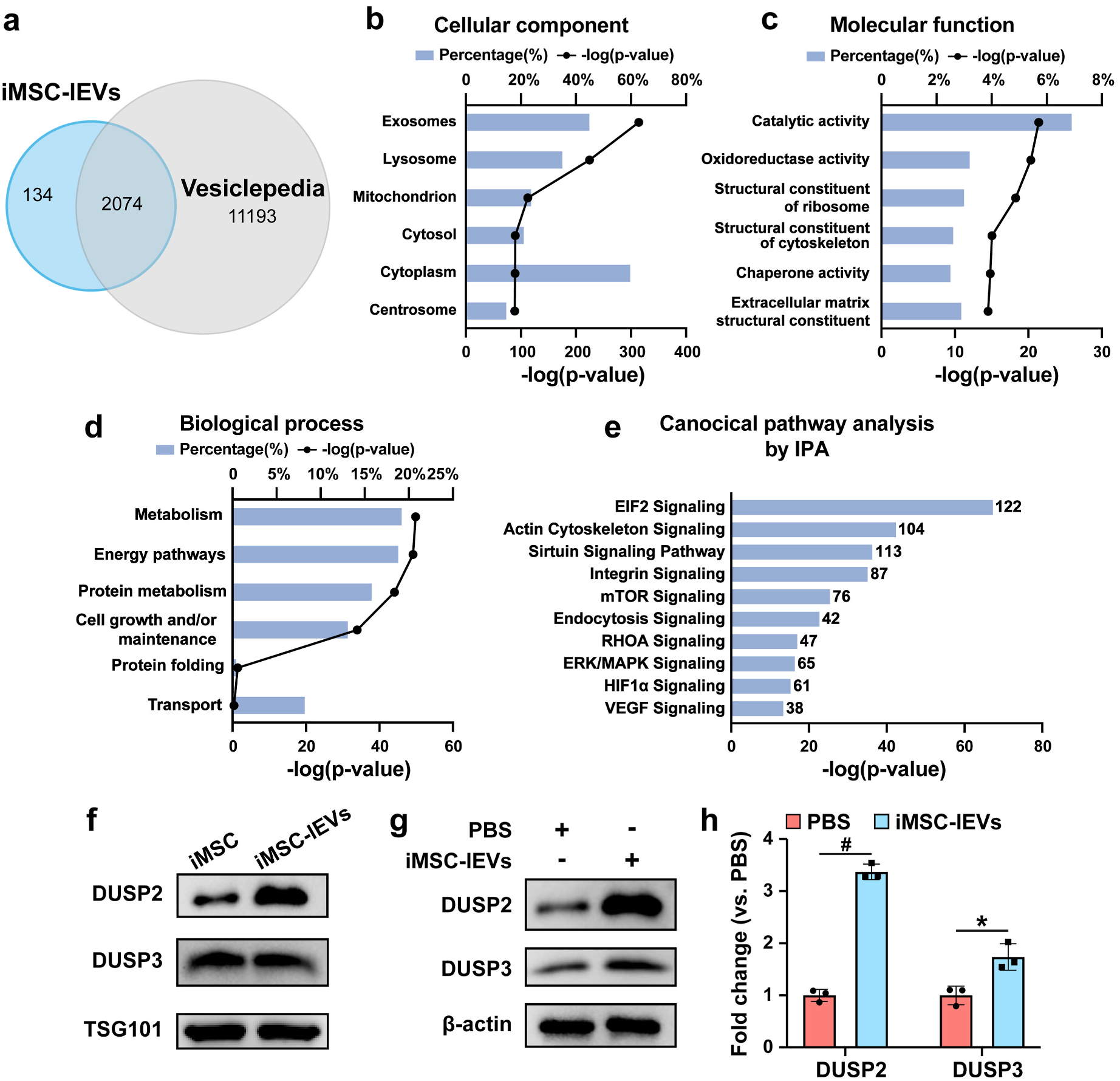
图6 iMSC-lEVs的蛋白质组学分析
6、iMSC-lEVs调节人肌腱组织中巨噬细胞的异质性和浸润性炎症细胞因子
进一步的,研究者探究iMSC-lEVs在肌腱病患者中的效果。选取肌腱病患者的肌腱组织,并与iMSC-lEVs体外培养。结果显示,iMSC-lEVs显著降低M1巨噬细胞的比例,并增加M2巨噬细胞的比例。此外,iMSC-lEVs能够降低炎性细胞因子IL-1β、tnf - α、IL-6和NGF的表达。这些数据与之前的动物实验结果一致,从而进一步证实iMSC-lEVs对人体肌腱组织的有效性。
小结:
文章作者证明iMSC-lEVs能够部分通过DUSP2和DUSP3介导p38 MAPK信号通路,使炎性巨噬细胞向抗炎巨噬细胞进行极化转变,从而减轻肌腱病变中的疼痛和炎症。这些发现揭示了iMSC-lEVs在免疫调节中的特殊作用,并强调了一种可改善肌腱病变和其他炎症疾病的新型有效的无细胞疗法。
